

WB结果不理想?实验步骤流程很重要!
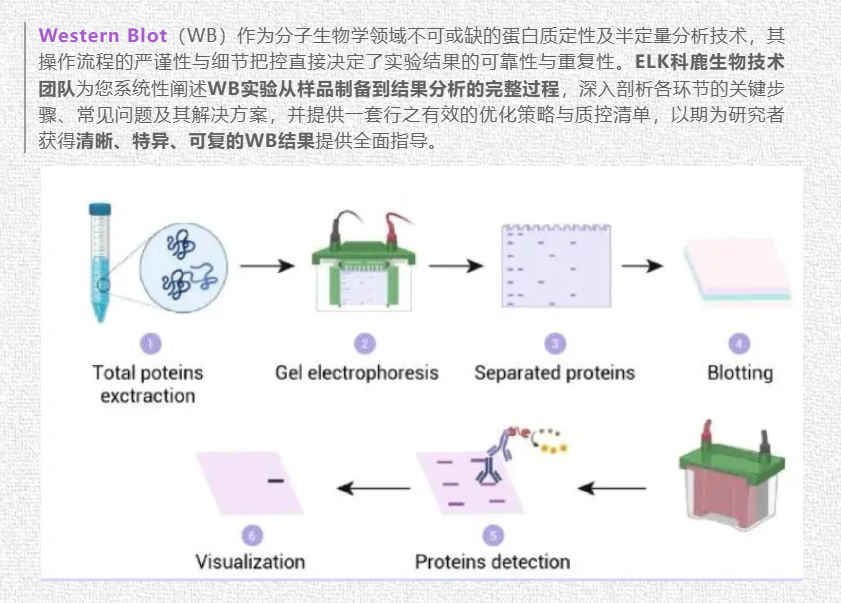
WB实验全流程详解与优化指南

第一阶段:样品制备——成功的基石
样品来源与处理:
细胞样品: 贴壁细胞需用预冷的PBS轻柔洗涤后,直接加入裂解液刮取;悬浮细胞离心收集后洗涤,再行裂解。操作全程保持低温,防止蛋白降解。
组织样品: 取材后应立即液氮速冻,-80°C保存,研磨时需在液氮或低温研磨仪中进行,确保组织充分破碎且低温。
裂解液的选择与配制:
常用裂解液: RIPA裂解液适用于大多数可溶性蛋白;NP-40裂解液更为温和,利于保留蛋白质间互作;对于难溶蛋白(如膜蛋白、核蛋白),可选用更强效的裂解液(如含SDS)。
抑制剂添加: 必须新鲜加入蛋白酶抑制剂 cocktail 和磷酸酶抑制剂(如检测磷酸化蛋白)。建议将抑制剂配制成高浓度储存液,分装冻存,避免反复冻融。
裂解条件: 冰上裂解30min,期间可间歇涡旋,随后,4°C,12000-14000 g离心15min,取上清。
蛋白定量与变性:定量方法: BCA法因其抗干扰能力较强而被推荐,所有样品应使用同一标准曲线测定,确保数据可比性。
上样缓冲液: 使用含还原剂(如β-巯基乙醇或DTT)和SDS的Laemmli Buffer,加热变性是关键步骤:通常95-100°C加热5-10min。
上样量优化: 常规上样量为20-50 μg总蛋白。对于低丰度蛋白,可增加至80-100 μg;高丰度蛋白则可减少至10-20 μg,需通过预实验确定最佳上样量。
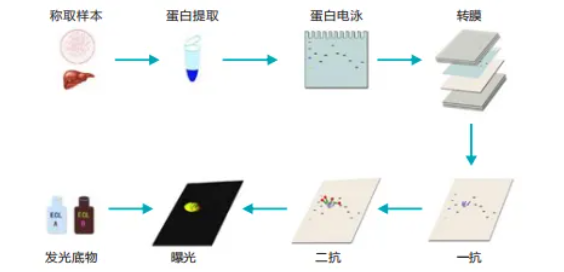
第二阶段:SDS-PAGE电泳——精密的分离
凝胶配制:
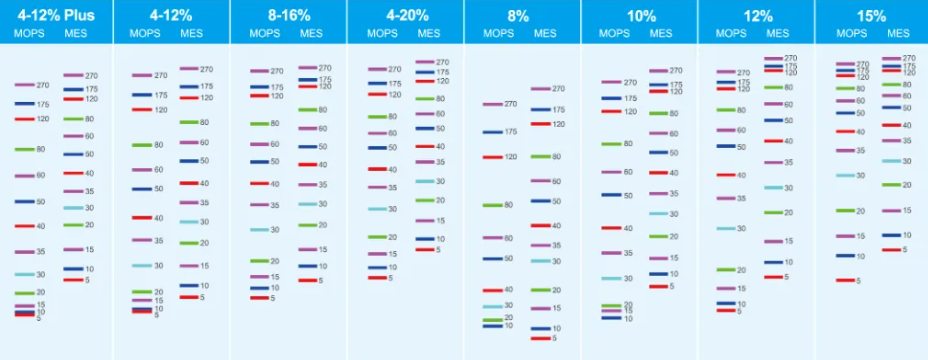
浓度选择: 根据目标蛋白分子量选择分离胶浓度,一般原则:6-8%胶用于>100 kDa蛋白;10%胶用于20-100 kDa蛋白;12-15%胶用于<20 kDa蛋白。梯度胶(如4-20%)适用于分子量分布广的样品。
制胶要点: 玻璃板需洁净;灌胶后及时用异丙醇或水压平界面;确保充分聚合(室温下至少静置45min);新制胶可于4°C湿润保存过夜,使用效果更佳。
上样与电泳:
上样技巧: 使用平头微量进样器针头;将样品缓慢加至孔底;两侧孔加入预染蛋白Marker;空白孔加等体积1×上样缓冲液。
电泳条件: 采用恒压模式。浓缩胶阶段:80-90 V,约30min或至溴酚蓝进入分离胶。分 离胶阶段:根据胶浓度调整为110-150 V。电泳过程中需注意降温,尤其在夏天,可将电泳槽置于冰水浴中。
内参选择: 常用内参包括β-actin(42 kDa)、GAPDH(36 kDa)、Tubulin(55 kDa)等。建议根据实验体系和目标蛋白分子量选择合适的內参,有时需使用两个不同分子量的内参互为佐证。
第三阶段:蛋白质转膜——高效的迁移
转膜是将分离的蛋白质从凝胶原位转移至固相支持物(膜)上的关键步骤。
转膜方式选择:
湿转: 通用性强,尤其适合大分子量蛋白,转膜效率高,但耗时较长(常为90min以上),缓冲液用量大。
半干转: 快速(15-45min),缓冲液用量极少,但对“三明治”结构的平整度要求极高,且容易发热,较适合小分子量蛋白。
膜的选择与处理:
NC膜(硝酸纤维素膜): 结合能力强,背景低,成本较低,但较脆,机械强度差。
PVDF膜: 机械强度高,可进行多次剥离(Strip)和重孵育,蛋白质结合容量大,但需在使用前用甲醇浸润激活。
膜的处理: 裁切膜的大小需略大于凝胶。PVDF膜在甲醇中浸泡15秒后,转入转膜缓冲液平衡。
“三明治”组装与转膜条件:
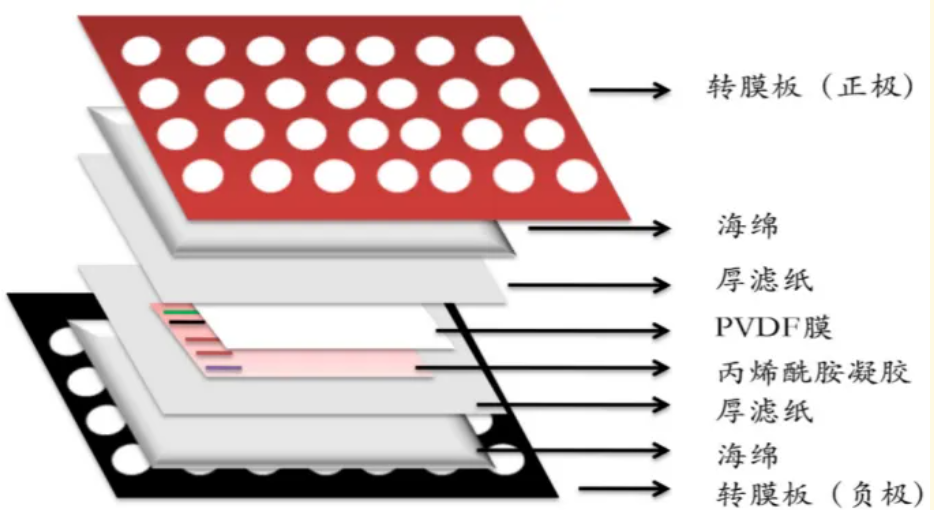
组装顺序(湿转,从正极到负极): 海绵→滤纸→凝胶→膜→滤纸→海绵。每一步都必须用玻璃棒或转印滚筒仔细赶走气泡,气泡是转膜失败的主要原因之一。
缓冲液: 湿转常用Towbin缓冲液(25 mM Tris, 192 mM甘氨酸,20%甲醇)。甲醇有助于蛋白与膜结合并防止凝胶膨胀,但会降低转膜效率,对大分子量蛋白可降至10%。
条件优化: 恒流转印。一般条件:250-300 mA,60-90min,置于冰浴或4°C冷房中。大分子量蛋白需更低电流、更长时间(如200 mA,过夜)。
第四阶段:免疫学检测——特异性的结合
封闭:
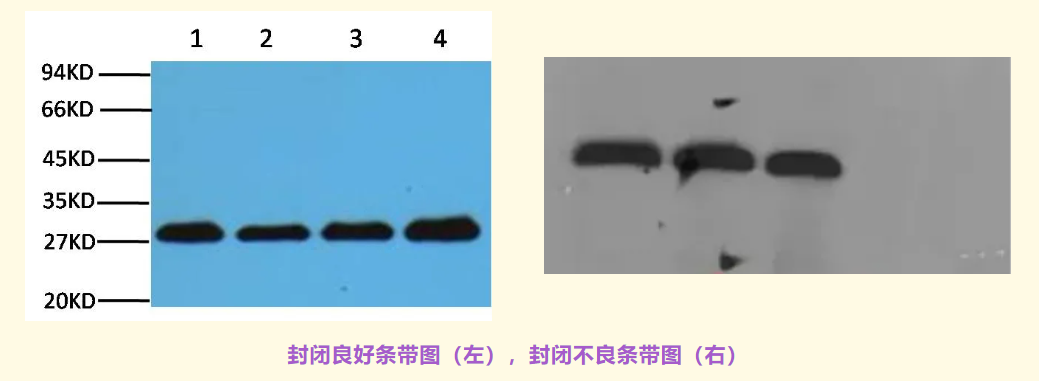
目的: 用非相关蛋白占据膜上未结合蛋白的空位,减少抗体非特异性吸附,降低背景。
封闭剂: 5% 脱脂奶粉(TBST配制)最为常用,成本低,但可能含有磷酸酶,影响磷酸化蛋白检测。5% BSA(牛血清蛋白)是检测磷酸化蛋白的首选,背景也更低。
条件: 室温摇床封闭1-2h,或4°C封闭过夜。
一抗孵育:
稀释: 严格按照抗体说明书推荐范围进行稀释,并使用含1% B特异性、低背景的结合。若时间紧迫,室温孵育2h亦可,但效果可能稍逊。
洗膜: 一抗孵育后,用TBST在室温摇床上洗涤3次,每次5min
二抗孵育:
选择: 根据一抗的种属来源选择对应的HRP(辣根过氧化物酶)或AP(碱性磷酸酶)标记的二抗,HRP-ECL发光系统最为普及。
稀释与孵育: 用封闭液或TBST稀释,室温摇床孵育1-2h。
洗膜: 用TBST在室温摇床上洗涤3次,每次5min,比一抗后洗涤更为关键,以彻底洗去未结合的二抗。
第五阶段:化学发光与成像分析——结果的呈现
化学发光:
底物配制: ECL发光液A液和B液按1:1比例混合,现用现配,均匀滴加在膜上,覆盖所有区域。
曝光: 在暗室或化学发光成像仪中进行,采用不同曝光时间多次采集图像,避免信号过饱和(条带中心发白)或曝光不足,可先进行短时间预览扫描。
图像分析:
软件: 使用ImageJ、Quantity One、Image Lab等软件进行分析。


在线咨询
Online consultation
-
在线咨询
-
技术支持

关注微信公众号




