

蛋白磷酸化:蛋白质活力和功能的重要调节方式
在生命科学的分子世界里,蛋白质是生命活动的直接执行者。然而,蛋白质并非静态的砖块,而是动态的分子机器。为了应对外界环境的瞬息万变,细胞演化出了一套精密的调控系统,其中蛋白磷酸化是最常见、最重要的一种翻译后修饰方式。它像一个无形的开关,通过快速、可逆的化学修饰,精确控制着蛋白质的活力、定位与功能,从而决定细胞的命运。
1. 什么是蛋白磷酸化?
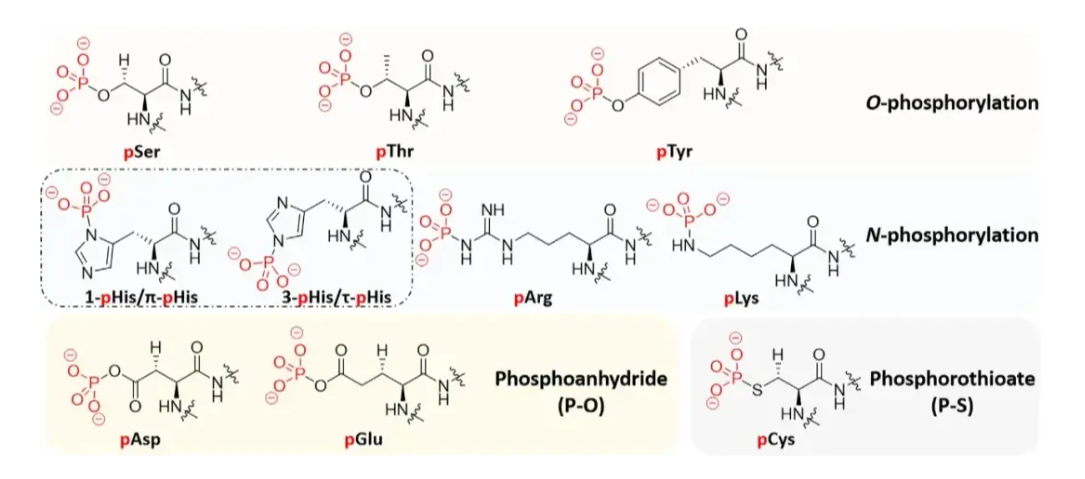
蛋白磷酸化是指在一类称为激酶的催化下,将ATP上的磷酸基团(PO₄³⁻)转移到底物蛋白质特定氨基酸残基上的过程。反之,将磷酸基团移除的过程则由磷酸酶介导。这种磷酸基团的添加与去除,如同给蛋白质贴上或撕去一个“标签”,能够迅速改变蛋白质的构象和活性。
在真核细胞中,磷酸化主要发生在丝氨酸(Ser)、苏氨酸(Thr) 和酪氨酸(Tyr) 残基上,其中丝氨酸磷酸化最为普遍。这三种经典的磷酸化方式构成了目前我们对细胞信号网络认知的基石。
2. 磷酸化如何调控蛋白质功能?
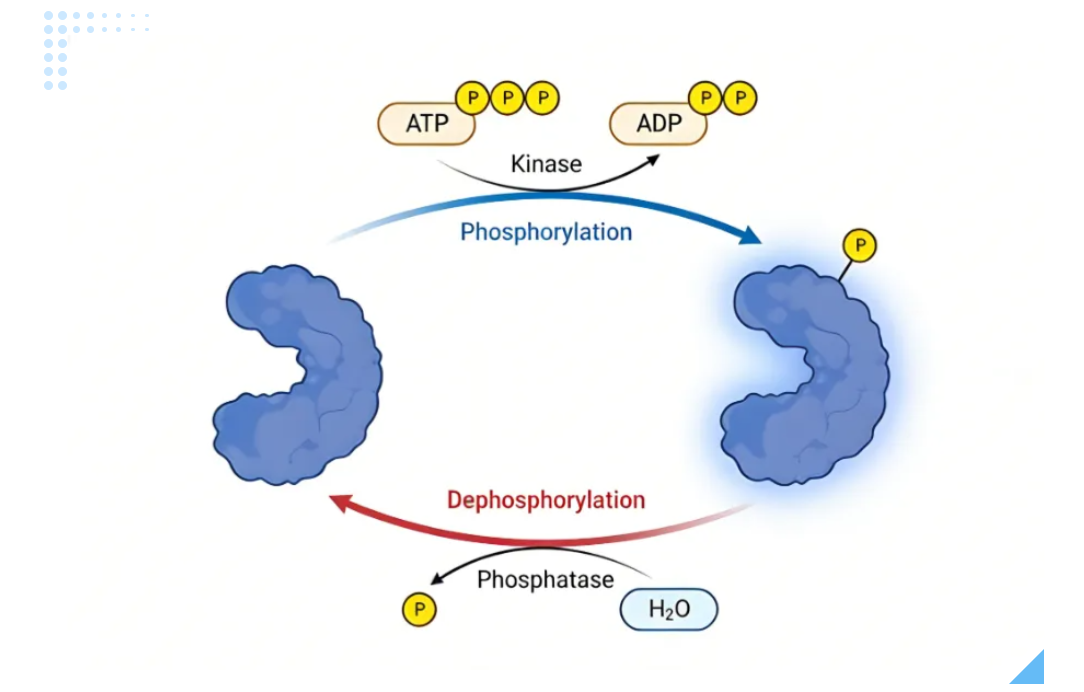
磷酸化对蛋白质功能的调节是多维度的,它不仅是简单的“开”与“关”,更是一种精妙的微调机制。
第一,直接调节酶活性。磷酸基团带有强烈的负电荷,引入蛋白质后可以诱导蛋白质三维结构的改变。例如,位于激酶活性中心的磷酸化往往能激活酶活性;而在非活性中心的磷酸化,则可能像一把锁一样抑制酶的活性。糖原合成酶激酶-3β(GSK-3β)在Ser9位点的磷酸化会抑制其活性,从而调控糖代谢。
第二,控制细胞定位。磷酸化可以作为“分子地址标签”,改变蛋白质在细胞内的分布。某些蛋白质在磷酸化后会被核膜上的受体识别,从而从细胞质进入细胞核执行转录调控功能;另一些则可能被锚定在细胞膜上。
第三,介导蛋白质互作。磷酸化残基可以成为其他蛋白质识别的“对接位点”。含有特定结构域(如SH2结构域或14-3-3蛋白)的蛋白质能够特异性识别磷酸化酪氨酸或丝氨酸/苏氨酸,从而招募下游信号分子形成复合物,级联放大信号。
第四,调控细胞周期与凋亡。细胞周期的精确运行依赖于周期蛋白依赖性激酶(CDKs)的周期性磷酸化事件。从G1期到S期的转变,再到有丝分裂的完成,每一步都受到磷酸化时钟的严格监控。一旦磷酸化失调,可能导致细胞周期失控,进而引发癌变。
3. 磷酸化的动态性与研究挑战
蛋白磷酸化具有几个显著特征,这也使其成为研究的热点和难点:
高度动态性:磷酸化状态可在细胞受到刺激后的几秒到几分钟内迅速发生变化,是对外界信号的即时响应。
低化学计量比:在某一时刻,只有一小部分蛋白质分子被磷酸化,这导致检测信号极其微弱。
位点特异性:同一个蛋白质上不同位点的磷酸化可能产生完全相反甚至截然不同的生物学效应。
因此,研究磷酸化通常需要依赖特定的技术策略。首先,由于磷酸化肽段在总肽段中占比极低(通常<5%),必须进行富集,常用方法包括 immobilized metal affinity chromatography (IMAC) 和二氧化钛(TiO₂)色谱。随后,借助高分辨率质谱进行鉴定,并通过定量蛋白质组学(如SILAC、TMT、ELISA技术)监测其动态变化。
4. 前沿进展:从经典到非经典磷酸化
尽管我们对丝氨酸/苏氨酸/酪氨酸磷酸化已经有了深入理解,但科学探索从未止步。近年来,磷酸化修饰的复杂版图正在以前所未有的速度扩展。
非经典氨基酸磷酸化:研究开始关注那些不太稳定但同样重要的修饰,如组氨酸磷酸化。组氨酸磷酸化在原核生物信号转导中占据核心地位,但在哺乳动物细胞中由于磷酸-组氨酸键的不稳定性(酸不稳定)长期被忽视。随着特异性富集方法和抗体的开发,科学家们正在重新评估其在真核生物中的作用 。
非常规修饰类型:除了单磷酸化,细胞中还存在着更为复杂的“超级磷酸化”现象。
焦磷酸化:由肌醇焦磷酸信使驱动,将已磷酸化的丝氨酸残基进一步磷酸化,生成二磷酸化的侧链。
多磷酸化与寡磷酸化:2025年发表在《Nature Chemistry》上的一项研究揭示了一种全新的模式——蛋白寡磷酸化。研究发现,核苷二磷酸激酶NME1能够利用ATP作为辅因子,在Thr94位点自我催化形成一个长达六个磷酸基团的寡磷酸链。这种修饰不仅完全抑制了NME1原有的激酶活性,还赋予了它全新的蛋白质相互作用能力。
此外,所谓的“暗激酶组”(dark kinome)——即那些功能尚未被充分研究的激酶,以及没有催化活性的假激酶和假磷酸酶,正逐渐被发现它们在信号网络中扮演着重要的调节角色。
5. 未来展望:多组学整合与精准医学
随着磷酸化蛋白质组学技术的成熟,单一组学的分析已无法满足揭示复杂生命过程的需求。未来的趋势是将磷酸化蛋白质组学与基因组学、转录组学、代谢组学进行多维度整合。
在多组学框架下,磷酸化数据扮演着“功能解码器”的角色。它能够解释为何虽然基因未突变,但蛋白功能却异常;它也能揭示药物到底是通过抑制哪条信号通路(如PI3K-AKT或MAPK)而起效的。通过结合机器学习预测激酶-底物关系和网络建模,研究者能够构建从“基因突变”到“信号失控”再到“疾病表型”的完整链条,从而发现更精准的药物靶点和生物标志物。
蛋白磷酸化作为一种古老而进化保守的调节机制,以其独特的简洁性和高效性,掌控着生命活动的万千变化。从最初的代谢酶活性调节,到复杂的信号转导网络,再到今天发现的寡磷酸化等全新修饰形式,我们对这一“分子开关”的理解仍在不断深化。深入解析磷酸化的密码,不仅是为了满足基础研究的好奇心,更是为了在癌症、神经退行性疾病、糖尿病等重大疾病面前,找到干预和治疗的钥匙。
在线咨询
Online consultation
-
在线咨询
-
技术支持

关注微信公众号




